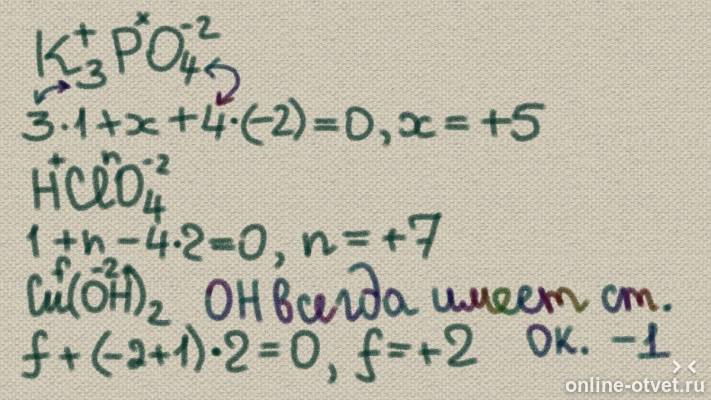Вопрос по химии:
Научите пожалуйста определять степени окисления в кислотах . и как определить индексы в (оксидах, основаниях, кислотах, солях)
Завтра контрольная, я думаю что справлюсь, но уже запуталась с этими степенями :( и особенно индексами.Помогите пожалуйста
Трудности с пониманием предмета? Готовишься к экзаменам, ОГЭ или ЕГЭ?
Воспользуйся формой подбора репетитора и занимайся онлайн. Пробный урок - бесплатно!
- 08.10.2017 09:11
- Химия
- remove_red_eye 4908
- thumb_up 20
Ответы и объяснения 1
Надеюсь, мои пояснения не покажутся очень сложными
В кислотах ион водорода (Н+) является всегда однозарядным, его степень окисления в кислотах и кислых солях всегда соответствует +1. В анионах кислот (всем остальным в кислоте кроме атомов Н) кислород всегда проявляет степень окисления -2. А уже отсюда по положению об электронейтральности молекулы и вычисляется степень окисления остальных элементов в соединении.
Уже из этих положений ясно, что имеют место особенные (часто встречаемые) степени окисления элементов. Чтобы найти им объяснение, достаточно рассмотреть электронную конфигурацию элемента, но сейчас не об этом. У фосфора чаще всего такие степени окисления - +3 и +5, у азота - +3, +5, -3, у серы - +4, +6, -2 и т. д.
В приложении рассмотрены пара примеров.
Не забывайте, что у катионов (металлы) степень окисления почти всегда равна номеру группы по таблице Менделеева. Натрий, калий, литий имеют степень окисления +1, магний, кальций и барий - +2, алюминий +3. Исключения составляют металлы d-периода (у них степень окисления можно лишь запомнить). Хром имеет степееь окисления +3, цинк и марганец - +2 и т. д.
- 09.10.2017 16:54
- thumb_up 48
Знаете ответ? Поделитесь им!
Есть сомнения?
Не нашли подходящего ответа на вопрос или ответ отсутствует? Воспользуйтесь поиском по сайту, чтобы найти все ответы на похожие вопросы в разделе Химия.
Трудности с домашними заданиями? Не стесняйтесь попросить о помощи - смело задавайте вопросы!
Химия — одна из важнейших и обширных областей естествознания, наука о веществах, их составе и строении, их свойствах, зависящих от состава и строения, их превращениях, ведущих к изменению состава — химических реакциях, а также о законах и закономерностях, которым эти превращения подчиняются.